老年性痴呆治疗艰难前行【科学】
很少有生活经历能比阿尔茨海默氏症的诊断更能引起人们的忧虑。直到20世纪80年代,它才为公众所知,在发达国家十大最常见的致命疾病中,它是唯一缺乏疾病改良治疗的疾病。阿尔茨海默氏症影响所有种族的人;在美国,非洲裔美国人的患病率是欧洲裔美国人的两倍。据推算,老年痴呆症(AD~ 60%)对社会造成的累计经济负担将超过心脏病和癌症。定义阿尔茨海默氏症神经病理的淀粉样斑块[淀粉样蛋白-β (Aβ)]和神经纤维缠结(tau)的关键蛋白的特性已经被确定。结合广泛的遗传学研究,提出了服务于记忆和认知的大脑网络损伤形成的序列。针对这些蛋白质的抗体已经进入了晚期试验阶段,而清除Aβ的aducamumab最近也获得了批准,尽管有争议。
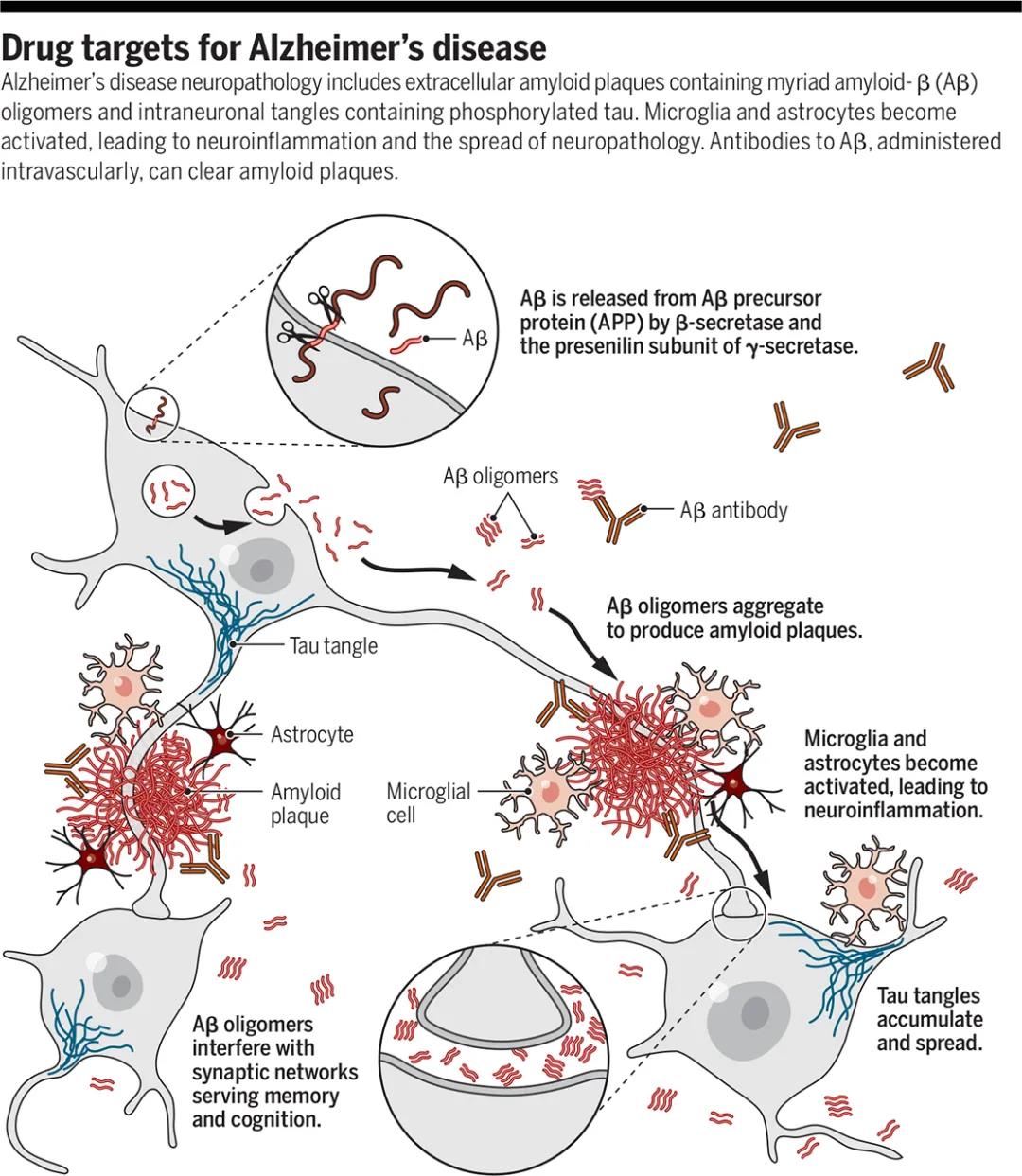
通过对APP (Aβ前体蛋白)和早老性蛋白(γ分泌酶的催化亚基,它切割APP生成Aβ)发生罕见致病突变的人类进行纵向分析,可以清楚地看到,大脑中的生化变化至少在认知症状出现之前20年就开始了。在这段漫长的症状前间隔期间,自聚集Aβ42肽在细胞外聚集,形成最初可溶的低聚体,然后逐渐增大的聚合物和不溶原纤维,这些低聚体与小胶质细胞、星形胶质细胞、无数神经突起和突触的细胞膜结合(见图)。虽然阿尔茨海默氏症的淀粉样蛋白假设通常是线性的,但许多变化可能发生在时间邻近。
典型晚发性阿尔茨海默氏症(65岁以后)的全基因组关联研究已经集中在胆固醇和脂质调节、突触网络功能,特别是小胶质细胞增生(改变的小胶质细胞)和神经炎症的不同基因的风险等位基因上。最有效的遗传危险因素是载脂蛋白E (APOE) ϵ4变体:杂合性使阿尔茨海默氏症风险增加2- 5倍,纯合性使其>增加5- 10倍。其致病机制似乎涉及胶质细胞介导的大脑细胞外间隙Aβ清除减少,导致大脑斑块和微血管中淀粉样蛋白增多。在小鼠中,APOE4蛋白也可以促进tau介导的神经变性和胶质细胞激活。其他一些阿尔茨海默氏症遗传风险因素也同样与增强的Aβ沉积和/或巨噬细胞和小胶质细胞对其的反应有关。
20年前,关于阿尔茨海默氏症发病机理的理论似乎在淀粉样蛋白和tau蛋白沉积的首要作用上存在分歧。这个错误的二分法已被越来越多的人一致认为,大脑中β聚合下降表明可溶性β单体在脑脊液(CSF)和不溶性斑块上淀粉pet(正电子发射断层扫描)扫描]开始早在人们注定要发展为胶质细胞介导紧随其后细胞外Aβ数量的增加导致聚集,包括可溶性低聚物,似乎增强了tau缠结的累积和颞叶内侧神经突的改变,这些病变常出现在没有阿尔茨海默氏症的老年人身上。这种tau蛋白在大脑中的积累和扩散(可能通过神经元间的连接)似乎对阿尔茨海默氏症的认知症状的发展是必要的。在APP转基因小鼠中,删除编码tau蛋白的基因不会改变淀粉样斑块,但显著减轻了它们的行为后果。因此,Aβ寡聚化似乎启动了阿尔茨海默氏症的神经病理学,导致神经突和细胞体中的tau蛋白改变,以及小胶质细胞增生和血液单核细胞渗入大脑。
许多潜在阿尔茨海默氏症修饰剂的试验中,未能达到主要和次要结果,可能有一种或多种解释:药物未能在大脑中实现稳健和选择性的目标参与;在临床阶段开始治疗,但治疗太迟而无效;动力不足的试验;对认知的不良副作用;以及错误使用判断标准。到目前为止,失败的试验的确切原因各不相同。但最近的一些试验似乎达到了主要终点或接近它们,也达到了一些次要终点。
迄今为止,疾病改变的最明确证据来自二级生物标志物终点,主要是淀粉样蛋白-pet测量的18个月内淀粉样斑块的显著减少。例如,这发生在aducanumab的两个3期试验中,aducanumab是一种Aβ单克隆抗体,于2021年6月7日获得美国食品和药物管理局(FDA)批准。其他的生物标志物变化包括脑脊液磷酸化tau蛋白浓度升高的降低和脑tau- pet信号的降低,但这些结果仅在少数aducanumab受体中测量。尽管淀粉样蛋白沉积的显著减少可以被视为疾病改变的生物学证据,但伴随而来的是认知测试的明显混合结果,一项aducanumab试验(EMERGE, NCT02484547)在最高剂量达到了预定的主要和次要终点,而另一项试验(ENGAGE,NCT02477800)没有实现。尽管累积剂量的差异和试验执行的不均衡已经被作为这种差异的解释,但FDA顾问委员会不相信并投票反对批准。尽管如此,FDA还是批准了“加速批准”,并引用了两项试验中淀粉样蛋白的显著降低,并预期这将导致较少的认知衰退。它还要求在营销开始时进行确认性试验。
关于aducanumab的争议应该在最近其他阿尔茨海默氏症免疫治疗试验的背景下加以考虑。单克隆抗体lecanemab的一项大型2期试验(旨在结合和清除Aβ原纤维和低聚物)实现了主要和次要终点,包括显著降低淀粉样斑块和显著减少认知衰退(10),并已推进到3期试验(NCT03887455)。另一种Aβ单克隆抗体gantenerumab在2期试验中产生淀粉样斑块减少,认知功能下降较少(11),目前正处于3期试验(NCT03443973)。此外,抗体donanemab目标low-abundance但aggregation-prone变体β的修改包含pyroglutamate-3氨基酸, 最近被一个中等规模的阶段2所示试验显著降低淀粉样负担,伴随着显著减缓下降的心理测试和日常活动。值得注意的是,多纳单抗在试验开始时(根据tau- pet判断)tau负担相对较低的患者中发挥了认知作用,而不是在tau浓度较高的患者中。根据tau蛋白负担对患者进行分层是明智的,可用于未来的抗a β试验。然而,不幸的是,tau-PET和淀粉样蛋白- pet都只能定量纤维沉积,而不能定量引起神经毒性的可溶性低聚物。
在18个月的试验中,这四种抗a β的抗体明确地清除了大脑区域中对认知至关重要的淀粉样蛋白沉积,并且伴随这种效果的是20 - 40%的认知衰退减缓。总的来说,这些数据代表了阿尔茨海默氏症领域最接近于一种疾病修饰方法。到目前为止,认知方面的好处并不大,评估它们对病人和照顾者的临床意义的挑战依然存在。但这一挑战在其他慢性病中也经历过,例如,当抗逆转录病毒药物齐多夫定首次获得批准时,对其最初有限的益处的争议。
治疗阿尔茨海默氏症疾病的药物,预计使用时间越长、使用时间越早,就能更有效地减缓认知能力的下降。事实上,在症状前治疗淀粉样蛋白阳性的个体更有可能有效。在阿尔茨海默氏症小鼠模型中,早期使用aducanumab治疗可减少Aβ沉积和生活后期的下游神经病理。通过第一次(尽管是适度的)治疗获得实际经验应该会鼓励开发更有效的第二代药物。
一夜之间,一种无法治愈的、最终会致命的疾病变成了为无数阿尔茨海默氏症患者提供治疗方案的复杂挑战。令人惊讶的是,aducanumab标签上的适应症最初是“阿尔茨海默病”,但在面临批评后,FDA很快将其改为轻度认知障碍和轻度阿尔茨海默氏症,这反映了3期试验的进入标准。阿尔茨海默氏症临床医生也可能需要淀粉样蛋白病理证据。后者可以通过淀粉样蛋白- pet成像来确定,但这并不广泛,因此将依赖脑脊液谱来记录Aβ42单体减少和磷酸化tau蛋白增加的特征,这一直被用于确认阿尔茨海默氏症。
临床医生面临的一个特殊挑战是考虑比试验中受损更严重的淀粉样蛋白阳性患者进行治疗。提供aducanumab的阿尔茨海默氏症实践应该建立透明的患者适格性指南,希望在不同部位之间有有限的差异。药物标签规定了剂量和输注间隔,但随着认知能力下降的减缓变得明显,治疗患者的时间标准将不断发展。难以置信的治疗的实际挑战将导致皮下注射的药物,可以方便在家里使用。顺便说一句,缓释皮下路径可能降低抗体的主要不利影响的发生β:焦脑水肿(ARIA-E),这是自限性的,四分之三无症状的那些患者可能是淀粉样间隙或在局部血管炎症反应。偶有微出血(ARIA-H)发生在少数接受aducanumab的ARIA-E患者中,这些患者似乎无症状。aducanumab的初始价格(约5.6万美元/年)非常高,需要由保险或国家医疗服务提供者支付。在实施第一个经批准的阿尔茨海默氏症治疗方案时,这些挑战和其他挑战需要深思熟虑的计划和足智多谋,但这正是患者和护理人员期待已久的过程。
最近一个关键的进展是可以检测阿尔茨海默氏症神经病理的血液测试。血浆检测tau蛋白的某些片段和磷酸化抗原表位显得特别有希望,因为在阿尔茨海默氏症症状患者中,tau蛋白的改变是随着Aβ积累而发生的。比较各种tau和Aβ血浆检测在诊断阿尔茨海默氏症和监测进展中的敏感性是必要的。加快血浆生物标志物的开发对于在全球范围内筛查无数患者是否符合阿尔茨海默氏症修饰药物的要求至关重要。
额外治疗方法是至关重要的。在小分子方法中,β分泌酶抑制剂已经被基于机制的副作用所挫败,尽管正在考虑更低的剂量。一个未被研究的类是γ分泌酶调节剂,它变构地改变早衰蛋白的构象,从而将APP加工从较长的淀粉样变形式(Aβ42, Aβ43)转变为较短的抗淀粉样变形式(Aβ37, Aβ38)。除了Aβ,研究重点是通过免疫疗法或反义寡核苷酸来减缓tau蛋白的积累。鉴于巨噬细胞和小胶质细胞参与阿尔茨海默氏症的强大遗传证据,调节巨噬细胞和小胶质细胞的病理反应是非常有趣的。预防阿尔茨海默氏症的非药物方法也必须进行,包括锻炼、睡眠卫生、地中海饮食以及智力和社交方面的丰富。
许多慢性疾病治疗历史上,最初治疗药物疗效有限,往往逐渐被更有效的药物稳步取代。新兴的免疫疗法减缓了阿尔茨海默氏症的生物学过程,但提供了适度的临床效益。aducanumab的批准可能提供了一个概念证明,可以迅速改进。它也可能使联合治疗成为可能,这在慢性病中是典型的。在治疗学中,就像在生活中一样,一个人必须先学会走,才能学会跑。




