释氢纳米材料减轻脂肪肝论文

在非酒精性脂肪肝病(NAFLD)的发病过程中,肝细胞代谢紊乱会导致不稳定铁池的形成,其中过量的铁配位化合物(如游离血红素、柠檬酸亚铁、乳酸亚铁)会通过Fenton样反应催化过氧化氢(H2O2)分解为羟基自由基(∙OH),导致氧化应激、脂质过氧化以及细胞铁死亡,促进肝脏代谢功能紊乱和NAFLD的恶化。氢分子(H2)作为一种新兴的绿色抗氧化剂,在铁卟啉催化加氢作用下可中和∙OH,抑制氧化应激的发生。而H2治疗的疗效与其给药的剂量高度相关,因此提高H2给药的效率对疗效保证至关重要。近日,山东第一医科大学秦树存教授和上海交通大学何前军教授团队合作在国际生物医学工程杂志《Biomaterials》(2023 IF: 14)上发表论文,报道了NAFLD铁池中的游离血红素可以催化H2O2/∙OH的氢化,阻断基于血红素的Fenton样反应,从而利用N-(3-triethoxysilylpropyl) gluconamid修饰硅化镁纳米片(MSN),开发一种新的肝细胞靶向氢传递系统(MSN-Glu),有效地阻断了血红素催化的肝病恶性循环(如图所示)。开发的MSN-Glu纳米药物具有较高的送氢能力、持续的氢释放和肝细胞靶向行为,改善肝脏的代谢功能,实现了高效的NAFLD预防,为炎症相关疾病的预防提供一个新启示。
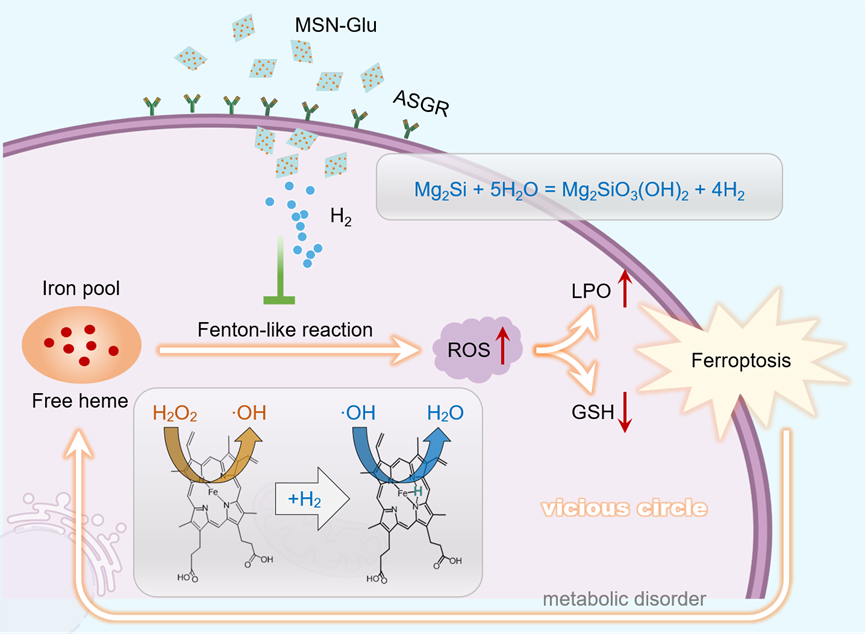
在此项研究中,体外实验和细胞实验充分证明了H2显著抑制血红素催化的Fenton样反应,降低体外∙OH和细胞中活性氧(ROS)的生成,同时提高细胞活性,表明H2可以通过催化铁池中的游离血红素来发挥抗氧化作用。MSN-Glu纳米片作为肝细胞靶向的氢供体,可通过主动识别肝细胞上的去唾液酸糖蛋白受体(ASGR),用于肝细胞靶向的H2传递。而且在生理条件下,H2持续释放时间长达8天,有利于高剂量H2输送,为抑制肝脏疾病的发展提供干预新手段。
基于肝细胞靶向H2释放行为,在NAFLD小鼠模型上也进一步验证了MSN-Glu对肝病的预防作用。利用胆碱缺乏的高脂肪饮食(CDAHFD,60 kcal%脂肪和0.1%蛋氨酸)建立与人类肝脏疾病发展相似的NAFLD小鼠模型,同时尾静脉注纳米材料进行干预。干预8周后,与模型组相比,注射MSN或MSN-Glu材料组的肝组织病理学、肝脏脂代谢紊乱、肝损伤以及炎症等方面均表现出显著的改善作用。而且进一步机制研究结果表明,MSN-Glu靶向细胞释放H2显著降低了肝脏中游离血红素、ROS和脂质过氧化物的蓄积,提高GSH水平和改善细胞器结构,抑制了铁死亡的发生和肝病的恶性循环。此外,该研究中的MSN-Glu纳米药物具有较高的生物相容性,其降解产物涉及H2、Mg2+和SiO32-,毒性低,易于在体内进行代谢,具有很高的临床转化潜力。该项工作涉及材料、化学、纳米技术、医学和生物学等多个领域,为预防炎症和氧化应激相关疾病提供新的思路。
文章第一作者赵敏,应届博士毕业生。




