微环境响应氢气材料增强肿瘤抑制研究【浙大】

1 引言
氢气(H₂)因其优异的安全性,已成为一种极具潜力的抗癌剂,能够重塑肿瘤微环境(TME)并诱导线粒体功能障碍介导的细胞死亡[1]。与常用治疗性气体(如一氧化碳[2]、二氧化硫[3]、硫化氢[4]、一氧化氮[5]等)相比,H₂具有出色的选择性抗氧化特性,可调控细胞信号传导与能量代谢[6],在有效抑制肿瘤增殖与转移的同时,减轻放化疗带来的不良反应。值得注意的是,H₂在治疗应用中表现出浓度依赖性的双重性:低浓度H₂可通过调控活性氧(ROS)发挥抗炎与细胞保护作用,而细胞内高浓度H₂则可能损伤线粒体呼吸功能并扰乱氧化还原稳态[7]。目前,氢疗策略主要聚焦于提高肿瘤内H₂积累量,以有效破坏肿瘤内氧化还原平衡、诱导肿瘤细胞死亡,进而改善抗肿瘤免疫应答。然而,氢基治疗仍受限于细胞内H₂生成不足、释放调控不佳及免疫应答增强效果有限等问题[8]。
当前的H₂递送方式包括直接氢气给药[9]、平台介导的氢气递送[10]以及瘤内原位产氢[11]。研究人员正致力于将高容量气体递送平台与氢疗结合,以提升抗肿瘤疗效。在这些策略中,基于金属氢化物的氢气递送平台因其设计灵活性,在抗癌治疗中展现出显著潜力[12]。然而,这类平台的临床转化面临诸多挑战,如合成过程复杂、水反应活性高及生物安全性欠佳[13]。除传统H₂递送策略外,肿瘤内原位产氢作为一种新兴的局部治疗策略,可实现H₂的可控、持续且靶向肿瘤的释放,同时生物毒性极低。但催化原位产氢通常需要外部触发信号,限制了其应用灵活性[14]。通过手术植入产氢镁基微电化学电池(MgG),可在局部产生高浓度H₂与金属离子,通过H₂扩散直接杀伤肿瘤细胞并调控肿瘤微环境[7]。尽管氢疗研究近年来取得进展,但关键挑战仍未解决,其中最核心的是肿瘤细胞内H₂释放效率低与治疗激活效果不佳,这阻碍了氢疗的广泛临床应用。解决这些局限需要创新性方案,核心在于实现细胞特异性与空间可控的细胞内氢气释放。这种精准递送不仅有助于阐明H₂在细胞环境中的调控机制,还能为优化H₂治疗平台提供设计框架。
本研究设计了一种基于锌掺杂还原型ZIF-8(沸石咪唑酯骨架材料-8)纳米颗粒(ReZIF-8)的pH响应型产氢纳米平台。ZIF-8的疏水多孔结构在生理pH条件下可保护锌(Zn)中心免受水相反应影响。ZIF-8由Zn²⁺与2-甲基咪唑(2-mIM)配体连接构成,形成多孔疏水骨架。2-mIM配体上的甲基可构建疏水微环境,通过空间位阻阻碍水分子渗透,从而防止Zn节点水解。关键在于,ReZIF-8的pH敏感性使其具有肿瘤微环境响应特性,在酸性条件下可选择性加速H₂生成与骨架降解。该机制可实现肿瘤组织及溶酶体腔内pH触发的精准产氢(方案1)。细胞内积累的H₂与Zn²⁺过载协同作用,严重破坏线粒体稳态,表现为线粒体膜电位显著去极化与细胞内ROS水平升高,最终导致ROS依赖性肿瘤细胞死亡[4,15]。此外,氢生成过程中pH响应性释放的免疫调节性Zn²⁺可显著增强肿瘤细胞死亡的免疫原性[13,16]。同时,H₂介导的信号级联反应可诱导恶性细胞终末分化并阻滞细胞周期。因此,ReZIF-8平台可实现“三模态”治疗效果:(1)局部氢介导的细胞毒性;(2)分化治疗;(3)免疫微环境重编程。这种由氢气触发的治疗级联反应(涵盖ICD诱导、细胞周期阻滞与肿瘤微环境重塑)与免疫检查点抑制具有显著协同作用,为癌症干预提供了一种新型氢基联合治疗策略。
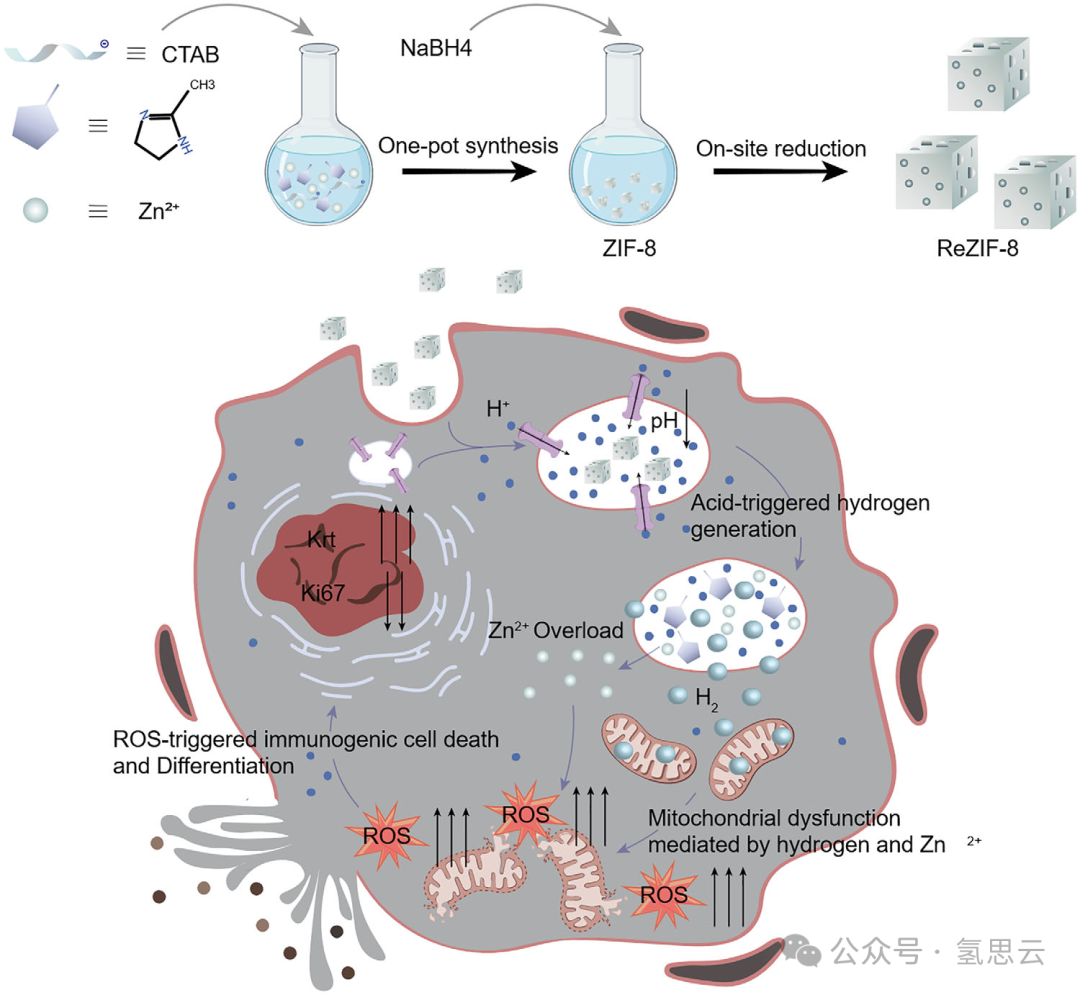
方案模式图
通过一锅法原位还原合成ReZIF-8及其诱导ROS刺激肿瘤细胞免疫原性细胞死亡的示意图。ReZIF-8凭借其表面正电位被肿瘤细胞有效内吞并定位于溶酶体。质子泵介导的质子内流导致溶酶体酸化,触发ReZIF-8的酸响应性降解,释放氢气与锌离子。这些物质共同诱导线粒体膜电位崩溃与细胞内活性氧(ROS)积累,从而激活肿瘤细胞的免疫原性细胞死亡。此外,ReZIF-8可通过氢气阻滞肿瘤细胞周期并促进细胞分化。




