修复线粒体的氢气反应器,用于感染骨再生!
发布时间:2026-03-30本文来源: 氢思云
用于感染性骨缺损修复中线粒体修复的氢气生物反应器
摘要
感染性骨缺损(Infected Bone Defects, IBDs)因反复感染和炎症反应,成为临床治疗中的重大难题。此类缺损以活性氧(Reactive Oxygen Species, ROS)爆发和线粒体功能障碍为特征,会形成氧化-炎症恶性循环,阻碍骨重塑过程。为解决这一问题,本研究构建了一种双网络水凝胶支架(QP-P/Mg),其由苯硼酸修饰的季铵化壳聚糖与甲基丙烯酸缩水甘油酯改性聚乙烯醇(QP-P)通过动态硼酸酯键和共价键交联而成,并负载镁微球(Mg spheres)。这种双交联网络赋予支架优异的可注射性和组织黏附性,同时整合了强效抗菌、ROS清除、促血管生成及成骨等多种功能。值得注意的是,镁微球可通过硼酸酯-镁离子(Mg²⁺)络合机制实现可控水解,持续释放氢气(H₂)和Mg²⁺:其中H₂可通过Nrf2/HO-1通路有效缓解氧化应激并恢复线粒体稳态,而Mg²⁺能够促进血管化骨再生。在大鼠感染性骨缺损模型中,QP-P/Mg支架实现了显著的骨再生效果,4周后骨体积分数(BV/TV)达45.32%±8.22%,较对照组提升6.27倍。这些结果表明,这种具有多功能特性的释氢水凝胶支架,可通过清除ROS和修复线粒体,促进感染性骨缺损的血管化骨再生,为感染性骨缺损的治疗提供了极具潜力的临床转化方向。
1. 引言
感染性骨缺损(IBDs)是由微生物引发的骨损伤,具有慢性炎症、愈合障碍及治疗难度大等特点[1,2]。口腔颌面部区域复杂的解剖结构和开放环境易导致反复感染,阻碍修复进程[3]。目前临床治疗方案通常为:先通过清创术和抗生素控制感染,再进行骨移植[4],但细菌清除率仅为60%~75%,复发率高达20%~30%[5]。此外,长期使用抗生素易引发耐药性和炎症并发症,而骨移植手术会增加再感染风险及社会经济负担[6,7]。感染性骨缺损的治疗挑战源于微生物侵袭、免疫防御与骨重塑失衡之间的复杂相互作用[8],其中活性氧(ROS)是最具破坏性的因素之一。入侵细菌与宿主免疫防御细胞会通过多种途径产生大量ROS[9],进而引发失控的ROS爆发,对局部微环境造成严重破坏。过量ROS会通过多种方式干扰线粒体功能,包括:通过脂质过氧化损伤线粒体膜、诱导线粒体通透性转换孔(mPTP)开放、抑制三羧酸循环以阻碍ATP生成、诱发线粒体自噬,以及通过产生8-羟基-2'-脱氧鸟苷或5-羟基胞嘧啶等氧化碱基损伤线粒体DNA(mtDNA)[10-12]。反过来,线粒体功能障碍会进一步加剧ROS生成,形成ROS爆发的恶性循环。
此外,ROS会放大局部炎症反应,导致骨重塑障碍[13,14]。免疫细胞产生的ROS可通过促进核因子κB(NF-κB)激活和NLRP3炎症小体囊泡释放,进一步加剧炎症反应,形成炎症与氧化水平持续放大的相互强化循环[15]。持续且失控的炎症会通过两种途径破坏骨稳态:一是通过免疫细胞分泌的核因子κB受体活化因子配体(RANKL)加速破骨细胞生成;二是通过抑制Wnt和IGF-1通路及下游成骨转录过程,降低成骨细胞活性[16,17]。不仅如此,炎症还会通过释放促炎细胞因子、基质金属蛋白酶(MMP)介导的细胞外基质降解,以及改变一氧化氮(NO)和P-选择素、血管细胞黏附分子-1(VCAM-1)等黏附分子导致内皮功能障碍,从而干扰血管生成[18],最终减少氧气和生物因子供应,阻碍骨再生[19]。因此,开发高效清除ROS的方法是成功修复感染性骨缺损的关键。
为改善以ROS为主导的感染性骨缺损微环境,本研究提出“感染控制-氧化应激缓解-组织再生”的治疗原则。氢气(H₂)因具有优异的线粒体膜穿透性、靶向清除毒性ROS的能力及极低的副作用,在激活线粒体功能、清除ROS方面展现出显著潜力。例如,已有研究表明,H₂可通过核因子红细胞2相关因子2(Nrf2)/血红素加氧酶-1(HO-1)通路及沉默信息调节因子1(Sirtuin 1)/过氧化物酶体增殖物激活受体γ共激活因子1α(PGC-1α)通路,高效缓解氧化应激,从而促进骨修复[20,21]。然而,H₂的快速释放特性限制了其应用。为解决这一问题,Chen等人设计了聚羟基脂肪酸酯包裹的CaSi₂纳米颗粒,通过减缓H₂释放,实现抗氧化、抗炎作用以重塑衰老微环境[22];Zhao等人则将氢气掺杂到TiO₂纳米棒中,利用光催化实现H₂的按需释放,以调节关节炎微环境[23]。
本研究构建了一种靶向ROS介导的感染性骨缺损修复的双网络水凝胶支架(QP-P/Mg)。该支架通过动态硼酸酯键和共价键,将甲基丙烯酸缩水甘油酯改性聚乙烯醇(PVAMA)、苯硼酸(PBA)修饰的季铵化壳聚糖(QCSPBA)与镁微球整合,赋予支架优异的可注射性、组织黏附性、抗菌性、抗氧化性、促血管生成及成骨性能。具体而言,QCSPBA上的PBA基团可与PVAMA上的羟基结合,形成可逆的动态硼酸酯键,使QP-P/Mg具有自修复和剪切变稀特性,从而具备可注射性,以适应形态不规则的感染性骨缺损[24];其次,PVAMA分子间的双键可形成共价交联网络,增强QP-P/Mg的强度和黏附性;第三,镁微球的水解过程受硼酸酯键与Mg²⁺络合作用的严格调控,可实现H₂和Mg²⁺的按需释放,同时避免pH值骤变。释放的Mg²⁺不仅能加速血管化和成骨再生[25-29],还可通过增加细菌膜通透性,与QCSPBA产生协同抗菌作用[30]。综上,QP-P/Mg系统可通过重建线粒体稳态,有效改善ROS过量的感染性骨缺损微环境,并在大鼠感染性骨缺损模型中展现出优异的成骨效果,为未来临床研究提供了潜在价值(图1)。
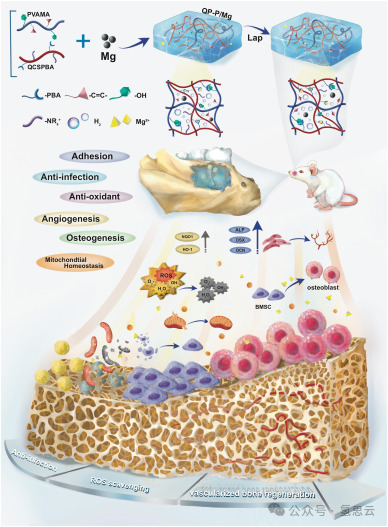
图1:QP-P/Mg水凝胶支架修复感染性骨缺损的设计策略及应用示意图
文献引用
Kong, Chunru, et al. "A H2-Releasing Bioreactor for Mitochondrial Rehabilitation in Infected Bone Defects Regeneration." Materials Today Bio (2025): 102295.
作者单位
Hospital of Stomatology, Jilin Provincial Key Laboratory of Tooth Development and Bone Remodeling, Jilin University, Changchun, 130021, China
上一篇:固态储氢实现电动化《科学》
已到最后一页




