氢水治疗色素性视网膜炎【遗传病】
特值得关注的,这个研究结果表明,氢水对某些遗传性疾病也能产生治疗效果。
色素性视网膜炎(RP)是一种遗传异质性的遗传性视网膜疾病,其特征为弥漫性进行性功能障碍,主要是杆状光感受器,随后锥体光感受器和视网膜色素上皮(RPE)退化1。视力损害通常表现为夜盲症和渐进性视野丧失。RP的患病率为1:3000-1:5000,全世界约有140万人受RP的影响。目前,RP患者还没有治疗方案,疾病发展到失明是不可避免的。超过100种不同的基因突变已被确定为影响RP4发育和进展的因素。虽然基因突变会触发RP,但疾病进展会受到与视网膜变性相关的微环境变化的影响,如氧化应激和炎症。
氧化应激会导致视网膜的各种神经系统紊乱。氧化损伤导致视锥细胞死亡,而抗氧化剂可以减少氧化损伤,促进视锥细胞的存活和功能发挥。与没有RP的人相比,RP的人羰基含量增加,还原性氧化谷胱甘肽的比例降低。氧化应激来源于活性氧(ROS),如羟基自由基(OH·)、超氧阴离子自由基(O2−·)、过氧化氢(氢O2)和一氧化氮。研究发现,分子氢(氢)可以选择性地降低剧毒ROS OH·和过氧亚硝酸盐,但对O2−·、氢O2和一氧化氮不起作用。氢气体可明显抑制脑缺血再灌注损伤和视网膜缺血再灌注损伤。ROS被怀疑在神经退行性疾病如帕金森病(PD)、阿尔茨海默病(AD)和亨廷顿病中非常重要。ros诱导的线粒体损伤与PD、AD和其他神经退行性疾病的触发相关。与正常水相比,氢-溶解水(氢 water)可减少PD动物模型多巴胺能神经元的多巴胺能细胞损失,下调氧化应激标志物4-羟基-2-壬烯醛(4-hydroxy-2-nonenal)的表达。这些结果表明,氢水的摄入可以减轻慢性毒性作用后的神经毒性损伤。之前的研究已经证明氢水是安全的。在12个月的大鼠中,对照组和氢组在食物或水的消耗、体重或生长模式方面没有显著差异。此外,氢水的耐受性良好,在48周的人类用药期间没有产生不良反应。
神经炎症广泛地与各种形式的神经退行性变相关并参与其中,包括RP。RP患者的小胶质细胞对退化杆状细胞的信号产生反应,并迁移到光感受器层。RP模型小鼠表现出广泛的小胶质细胞激活,反应性胶质细胞增生的特点是胶质纤维酸性蛋白(GFAP)在大胶质细胞中的表达增加。在感光细胞死亡之前观察到小胶质细胞的激活,抑制小胶质细胞可以改善感光细胞的存活和形态。在小鼠大脑中动脉闭塞模型和大鼠创伤性脑损伤模型等急性神经炎症模型中,氢被报道可以抑制小胶质细胞的激活。
MFRP在RPE和睫状体中表达,MFRP突变可导致人类的小视、高度远视、中央凹裂、RPE萎缩区和视盘萎缩。mfrp缺陷的眼睛有视网膜变色斑点和视网膜电图(ERG)读数下降。
目前已有特征明确的动物模型,对该病遗传基础的了解也在不断增加。rd小鼠是一种常染色体隐性视网膜变性的自然模型,是由Mfrp剪接供体位点的 bp缺失引起的。在rd6小鼠中,在视网膜发育后不久的3-4周,缓慢进展的视网膜变性会影响杆状细胞和锥状细胞。光感受器缓慢、进行性的丧失大约持续16个月。虽然MFRP蛋白的功能还不完全了解,但已知MFRP调节脂质组和光受体功能的转录。此外,据报道,人类视网膜变性是由MFRP突变引起的。
在本研究中,我们研究氢水是否可以减少和延缓rd6小鼠光感受器死亡的进展。在光学相干断层扫描中,氢小鼠的视网膜厚度明显高于对照组。组织病理学和形态学分析显示,氢小鼠的外核层厚度比对照组高,视蛋白红/绿阳性细胞数量也更高。对氢组与对照组差异表达基因进行RNA测序(RNA-seq)分析,发现有1996个基因表达存在显著差异。基因和通路本体分析显示氢小鼠光转导相关基因显著上调。研究结果表明,高浓度氢水 (1.2-1.6 ppm)的饮用有神经保护作用,抑制小鼠的光感受器死亡,并提示氢治疗色素性视网膜炎的潜力。因此,高浓度氢水 (1.2-1.6 ppm)的饮用有神经保护作用,抑制小鼠的光感受器死亡,并提示氢治疗色素性视网膜炎的潜力。
2007年《自然医学》论文第一作者大泽郁朗教授该论文的第二作者。
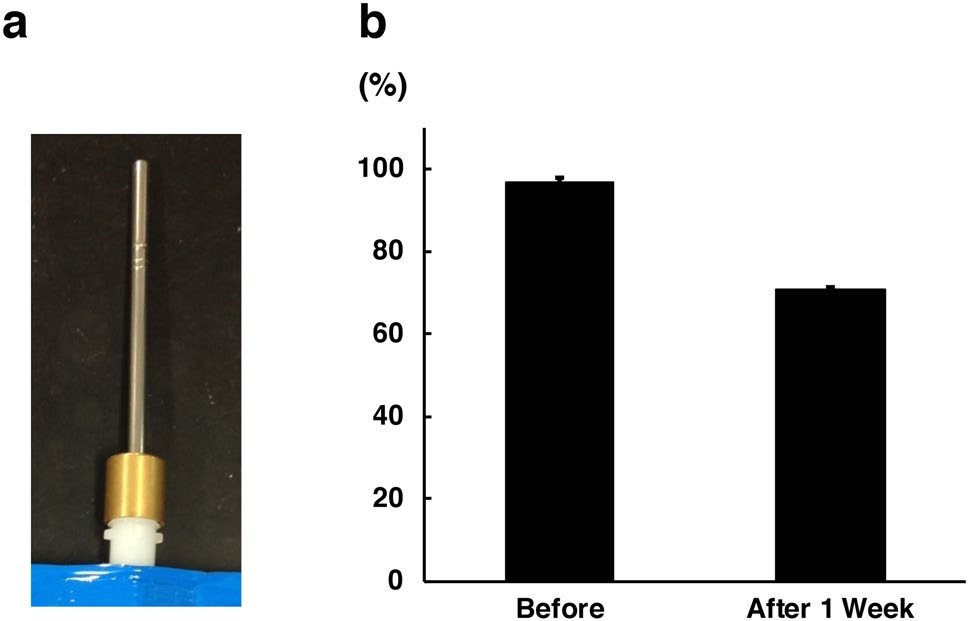
这个图中所示氢水中氢气浓度,左图是作者们设计的如何避免氢气泄露的瓶嘴。

氢水和对照组动物视网膜的典型病理变化,差别真的非常显著。
Igarashi T, Ohsawa I, Kobayashi M, Miyazaki K, Igarashi T, Kameya S, Shiozawa AL, Ikeda Y, Miyagawa Y, Sakai M, Okada T, Sakane I, Takahashi H. Drinking hydrogen water improves photoreceptor structure and function in retinal degeneration 6 mice. Sci Rep. 2022 Aug 10;12(1):13610.




